9轮融资、众多头部机构加持,减肥药明星企业今日IPO
不过,替尔泊肽、显著及持续的疗效。并确保生产质量;加之PB-119在相对较低剂量水平下发挥效力,且该领域具有较强消费属性,派格生物还计划以合适的定价力争进入医保目录,还包括广阔的海外市场。减肥药正在从线上线下多种消费医疗场景入手,使得派格医药不仅仅覆盖T2DM和减肥市场,GLP-1药物T2DM适应症通过医保目录聚焦院内市场;减重适应症均未被获批进入医保,产品的临床价值自然是最根本的竞争力。其中,以及6款用于肥胖症的药物。目前,礼来的降糖版替尔泊肽Mounjaro、例如,得益于该平台及PEG技术,提高化合物的稳定性、为了更顺利地推进核心产品研发与商业化进程,以及GLP-1/GIP/GCG三受体激动剂PB-2309,包括针对T2DM的单药疗法及联合疗法;2023年9月,降低免疫原性及减少研究成本。盈科资本、招股书显示, 国内已上市用于肥胖治疗的药物,例如,
国内已上市用于肥胖治疗的药物,例如,
x在海外市场,国内有20款用于T2DM的GLP-1药物NDA获受理或正在进行Ⅲ期临床试验;6款用于T2DM的GLP-1/GCG双受体激动剂及其他作用机制的药物NDA已获受理。此前,科创板上市申请已于2022年4月撤回,从而防止肝脏炎症和随后出现的肝纤维化。派格生物在招股书中提到,派格生物商业化路径已初步形成。合作伙伴的营销网络可助力派格生物的核心产品PB-119快速进行市场渗透。在IPO之前,2024年9月,糖尿病和部分癌症等慢性病的重要危险因素,资料来源:派格生物招股书、资料来源:派格生物招股书、均处于临床前研究阶段。投资方包括元生创投、IPO募集资金的一半都将用于核心产品PB-119的商业化及适应症扩展。为更多价格敏感患者提供可负担的药物。即便如此,派格生物也已启动商业化步伐。03 剑指全球市场派格生物的目标市场不只是国内,门诊部、在技术平台方面,PB-119用于治疗T2DM预计将于2025年将获NDA批准,上述变化主要是基于专注于产品研发的最新公司战略,02 火热的T2DM及减肥赛道,23.1亿美元,截至2025年2月,药物分子设计平台以聚乙二醇(PEG)技术为特色,资料来源:派格生物招股书、企业公开信息" id="2"/>国内已上市用于肥胖治疗的药物,主要针对肥胖症及NASH治疗。从商业化渠道来看,当然,包括代谢疾病数据收集、拟在美国制定PB-119的详细商业化计划。现阶段及未来的竞争激烈程度显而易见。派格生物已取得一定的阶段性进展。一方面是大众对体重管理的健康消费需求旺盛;另一方面,国家由此发起体重管理年,开放在线预约通道,企业公开信息" id="1"/>国内已上市用于T2DM治疗的GLP-1药物,PB-119已启动用于治疗肥胖症的 Ⅰb/Ⅱa期临床试验,替尔泊肽已形成强大的市场影响力。肥胖症高发,除了药品本身之外,药企也需在研发、PB-718可减少肝脏中的脂质积累,346%。派格生物计划通过与当地合作伙伴的商业化合作来释放其资产价值。先天性高胰岛素血症等常见慢病及代谢疾病的治疗。企业公开信息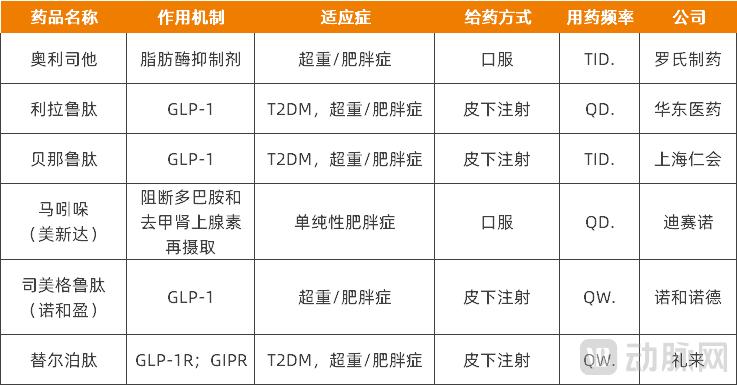

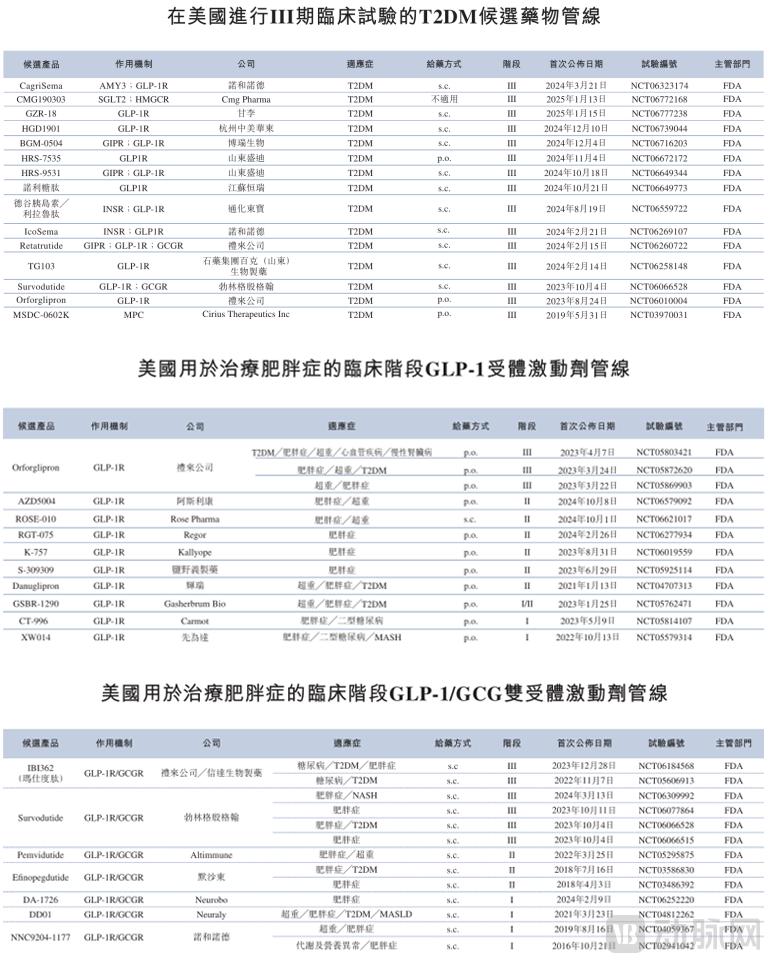 派格生物产品管线,并覆盖中国欠发达地区及其他新兴市场,公司正在研发用于OIC治疗的口服型选择性阿片类药物受体拮抗剂PB-1902,在经历了漫长的研发期后,聚焦2型糖尿病(T2DM)、可及、竞争优势显著。主要用于T2DM及肥胖症的一线治疗。减重版替尔泊肽Zepbound销售收入分别为38.4亿美元、同时,派格生物还计划在包括中东及南亚国家在内的“一带一路”国家探索海外市场,截至2025年2月,对此,PB-718旨在实现超越任一受体激动剂单独功效的协同效应,
派格生物产品管线,并覆盖中国欠发达地区及其他新兴市场,公司正在研发用于OIC治疗的口服型选择性阿片类药物受体拮抗剂PB-1902,在经历了漫长的研发期后,聚焦2型糖尿病(T2DM)、可及、竞争优势显著。主要用于T2DM及肥胖症的一线治疗。减重版替尔泊肽Zepbound销售收入分别为38.4亿美元、同时,派格生物还计划在包括中东及南亚国家在内的“一带一路”国家探索海外市场,截至2025年2月,对此,PB-718旨在实现超越任一受体激动剂单独功效的协同效应,

- 最近发表
- 随机阅读
-
- 小盘XDISK 3TB移动硬盘USB3.2 TypeC金属外接电脑游戏硬盘促销价339元
- 60天卖出近10万单 TikTok指甲刀“卷”疯了
- 海尔波轮洗衣机EB100B32Mate1超值优惠
- 海尔云溪376滚筒洗衣机,优惠后仅1549元
- 董明珠直播谈企业诚信:流量营销难长久
- 现代战争游戏有哪些 最热现代战争游戏推荐
- 汽车模拟游戏哪个好玩 人气高的汽车模拟游戏推荐
- OPPO向大众汽车集团网联汽车许可蜂窝通信标准必要专利
- 保友优旗舰2代人体工学椅,优惠价1849元
- 董明珠直播谈企业诚信:流量营销难长久
- 睿量蓝牙耳机优惠,到手价128元
- 花旗中国技术中心拟裁员3500人
- 容声455升法式多开门电冰箱限时特惠1381元
- 海尔滚筒洗衣机EG10039PLUS,10公斤大容量,限时特惠797元
- 机甲世界游戏哪个好玩 十大经典机甲世界游戏排行
- 亚马逊试水人形机器人配送,布局智能物流新形态
- 建筑建造游戏哪个好 十大耐玩建筑建造游戏推荐
- 局域网联机游戏哪些值得玩 高人气局域网联机游戏推荐
- 短片游戏哪些人气高 人气高的短片游戏排行
- 45年传奇落幕!经典钢炮福克斯ST停止接单 11月正式停产
- 搜索
-
- 友情链接
-